§ 22. Соли — продукты замещения атомов водорода в молекулах кислот на металлы
1. Какие вещества относятся к солям?
К солям относятся вещества, которые состоят из атомов металлов и кислотных остатков.
2. Из предложенного ряда выберите формулы солей: H2O, KNO3, Fe2O3, FeSO4, Na2CO3, H2SO4, K3PO4, CuO, СаCl2.
KNO3, FeSO4, Na2CO3, K3PO4, СаCl2
3. Назовите следующие соли: Na2CO3, Fe(NO3)2, CuCl2, Na2SO4, AlPO4, AgCl, Fe2(SO4)3, CaCO3.
Na2CO3 – карбонат натрия; Fe(NO3)2 – нитрат железа(II); CuCl2 – хлорид меди(II); Na2SO4 – сульфат натрия; AlPO4 – фосфат алюминия; AgCl – хлорид серебра; Fe2(SO4)3 – сульфат железа(III); CaCO3 – карбонат кальция.
4. Составьте формулы солей, в которых содержится кислотный остаток серной кислоты и атомы следующих металлов: цинк, натрий, железо(III).
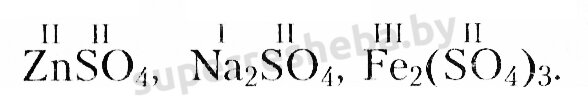
5. Вещество MgSO4 применяется в медицине, в производстве бумаги, в текстильной промышленности. Предложите способ получения этого вещества и напишите соответствующее уравнение реакции.
Один из способов получения MgSO4 – это взаимодействие магния с серной кислотой:
Mg + H2SO4 → MgSO4 + H2↑
6. Расставьте коэффициенты в предложенных схемах. Выберите из них схемы реакций замещения и назовите образующиеся соли:
а) 2Zn + O2 = 2ZnO;
б) 2Al + 6HCl = 2AlCl3 + 3H2↑ — реакция замещения;
в) 2H2O = 2H2↑ + O2↑;
г) Fe + H2SO4 = FeSO4 + H2↑ – реакция замещения.
7. Составьте уравнения и укажите типы химических реакций, с помощью которых можно осуществить следующие превращения:
а) HCl → H2 → H2O → O2 → CuO → Cu;
Ответ:
2HCl + Zn = ZnCl2↑ + H2 ↑ – реакция замещения;
2H2 + О2 = 2H2O – реакция соединения;
2H2O = 2H2↑ + O2↑ – реакция разложения;
O2 + 2Cu = 2CuO – реакция соединения;
CuO+ H2 = Cu + H2O – реакция замещения.
8. В смеси хлорида натрия и нитрата калия общей массой 120 г массовая доля NaCl в четыре раза меньше массовой доли KNO3. Рассчитайте массу хлорида натрия в указанной смеси.
Дано:
Найти:
Решение:
Пусть масса NaCl в смеси равна г. Тогда масса KNO3 будет равна:
Из условия задачи следует, что масса NaCl в 4 раза меньше массы KNO3. Запишем это в виде уравнения:
Масса хлорида натрия в смеси равна 24 г.
Ответ: 24 г.