Лаб. 9
1. В двух пробирках вам выданы растворы фосфата натрия и дигидрофосфата кальция. К растворам по каплям добавляйте реактивы хлорид бария и нитрат серебра. Занесите в таблицу результаты исследования.
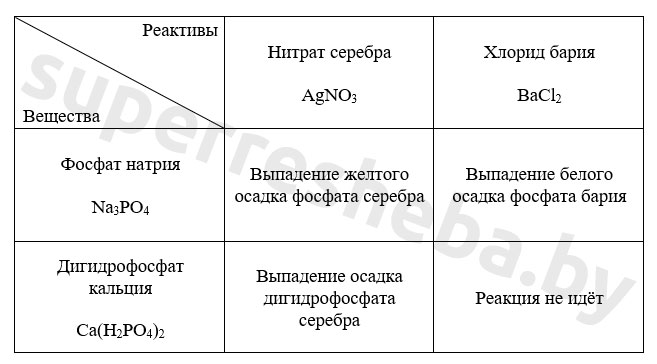
Уравнения реакций в молекулярном и ионном виде:

Вывод
1.
Для обнаружения фосфат-ионов можно брать любые вещества, которые будут образовывать осадок, в составе которого будет фосфат-ион. Например, и другие.
2.
Суть реакции в том, что, при взаимодействии в растворе фосфат-иона с ионом серебра, образуется нерастворимый осадок фосфата серебра желтого цвета.
2. Задания.
1.
— хлорид; — иодид.
— фосфат; — гидрофосфат.
2.
хлорид кальция, гидроксид натрия, нитрат серебра, карбонат калия.
3.
4.
5.
2 стадия:
3 стадия: